取0.486g金属镁,跟100ml适当浓度的稀硫酸完全反应(没有硫酸剩余)。求稀硫酸和生成硫酸镁溶液的物质的量浓度(溶液体积的变化忽略不计,镁原子量取24.3)。
正确答案:
化学反应方程式
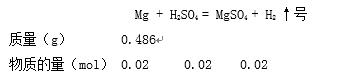
因为1mol金属镁与1mol硫酸反应生成1mol硫酸镁,可见100ml稀硫酸中含硫酸0.02mol;反应后100ml硫酸溶液中含硫酸镁0.02mol。
设稀硫酸的浓度为xmol·L-1,硫酸镁溶液的浓度为ymol·L-1,则
x=0.02×1000/100=0.2mol·L-1
y=0.02×1000/100=0.2mol·L-1
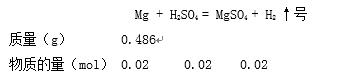
因为1mol金属镁与1mol硫酸反应生成1mol硫酸镁,可见100ml稀硫酸中含硫酸0.02mol;反应后100ml硫酸溶液中含硫酸镁0.02mol。
设稀硫酸的浓度为xmol·L-1,硫酸镁溶液的浓度为ymol·L-1,则
x=0.02×1000/100=0.2mol·L-1
y=0.02×1000/100=0.2mol·L-1
答案解析:有

微信扫一扫手机做题
