通C12于消石灰中,可得漂白粉,而在漂白粉溶液中加入盐酸可产生C12,试用电极电势说明这两个现象。
正确答案:

当C12通入消石灰溶液中时是碱性介质, C12可发生歧化反应:
C12可发生歧化反应:
2C12+2Ca(OH)2=Ca(C1O)2+CaC12+2H2O
得到的产物是漂白粉。加盐酸到漂白粉溶液中,使体系酸化,此时,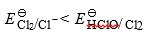 ,C12不能发生歧化反应,可发生的反应是C12歧化反应的逆反应:
,C12不能发生歧化反应,可发生的反应是C12歧化反应的逆反应:
Ca(C1O)2+4HCl=2Cl2+CaC12+2H2O
所以,上述两个反应是介质酸碱性的变化导致某些氧化还原反应方向改变的例证。

当C12通入消石灰溶液中时是碱性介质,
 C12可发生歧化反应:
C12可发生歧化反应:2C12+2Ca(OH)2=Ca(C1O)2+CaC12+2H2O
得到的产物是漂白粉。加盐酸到漂白粉溶液中,使体系酸化,此时,
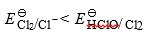 ,C12不能发生歧化反应,可发生的反应是C12歧化反应的逆反应:
,C12不能发生歧化反应,可发生的反应是C12歧化反应的逆反应:Ca(C1O)2+4HCl=2Cl2+CaC12+2H2O
所以,上述两个反应是介质酸碱性的变化导致某些氧化还原反应方向改变的例证。
答案解析:有

微信扫一扫手机做题
